C.T.P Fernando Volio Jiménez.
Área: Química.
Profesor: Emiliano Murillo M.
Alumnos: Aarón Hidalgo Villegas.
Andrés Arias Quesada.
Sección: 11-1.
Especialidad: Electrotecnia.
Año: 2017.
Teoría de
enlace de valencia:
Teoría del enlace de valencia (TEV) explica
la naturaleza de un enlace químico en una molécula, en términos de las valencias atómicas. La teoría del enlace de valencia se resume en la
regla de que el aromo central en
una molécula tiende a formar pares de electrones, en concordancia
con restricciones geométricas, según está definido por la regla del octeto. La teoría del
enlace de valencia está cercanamente relacionada con la teoría de los orbitales moleculares.
Teoría
del orbital molecular:
Es
un método para determinar el enlace quimico en el que los electrones no están asignados a enlaces
individuales entre átomos, sino que se mueven bajo la influencia de los núcleos
de toda la molécula.
En esta teoría, cada molécula
tiene un grupo de orbitales moleculares, y se asume que la función de onda ψf del
orbital molecular está escrita de manera aproximada como una simple combinación lineal de los números de orbitales
atómicos constituyentes χi, de acuerdo con la siguiente
ecuación:

Enlace iónico:
En Química, y en Física un enlace iónico o electrovalente es la unión
de átomosque resulta de la
presencia de atracción electrostática entre los iones de distinto
signo, es decir, uno fuertemente electropositivo (baja energía de ionización) y otro fuertemente electronegativo (alta afinidad electrónica). Eso se da cuando en el enlace, uno de los átomos capta electrones del otro. La
atracción electrostática entre los iones de carga opuesta causa que se unan y
formen un compuesto químico
simple, aquí no se fusionan; sino que uno da y otro recibe. Para que un enlace
iónico se genere es necesario que la diferencia (delta) de electronegatividades
sea mayor que 1,7 o igual.
Características:
·
Sus
enlaces son muy fuertes (depende fuertemente de la naturaleza de los iones).
·
Sólidos a temperatura ambiente
y poseen una estructura cristalina o
transparente en el sistema cúbico.
·
Son enlaces resultantes de la interacción entre
los metales de
los grupos I y II y
los no metales de los grupos VI y VII.
Los enlaces químicos se
forman ganando,
cediendo o compartiendo electrones para alcanzar
configuraciones electrónicas estables como por ejemplo las de los gases nobles.
Propiedades de los compuestos iónicos:
·
Son sólidos a temperatura ambiente.
·
Tienen altos puntos de fusión y ebullición.
·
Son solubles en solventes polares como el agua
·
Forman redes cristalinas altamente ordenadas.
·
Presenta una alta dureza y además son muy frágiles.
Enlace Covalente:
Son enlaces que se forman
cuando se comparte uno, dos o más paredes de electrones entre dos o más átomos.
Características:
·
Se forman con elementos no metálicos, se puede
formar por dos o tres no metales.
·
Enlace que se basa en compartir electrones, por lo
cual no se pierde ni se gana electrones.
·
Los elementos pueden unirse por enlace sencillo,
doble o triple.
Ejemplo:
·
Cloro
·
Agua
·
Oxigeno
·
Metano
·
Propano
En qué consisten las excepciones a la regla
del octeto:
Se presentan cuando un átomo sobre pasa el número de
electrones o le falta número de electrones en su última capa, es decir, tiene
más de 8 e- o tiene menos de 8 e-. Es una excepción a la regla del octeto porque
alcanza la estabilidad con seis electrones en la capa de valencia.
Tipos de enlaces
Covalentes:
·
Enlace
covalente no polar:
Se presenta entre átomos del
mismo elemento o entre átomos con muy poca diferencia de electronegatividad.
·
Enlace
covalente polar:
En la mayoría de los enlaces covalentes, los átomos tienen diferentes
electronegatividades, y como resultado, un átomo tiene mayor fuerza de
atracción por el par de electrones compartido que el otro átomo.
·
Enlace
covalente coordinado:
En lugar de
aportar un electrón cada átomo del enlace, los dos
electrones son aportados por el mismo átomo.
·
Enlaces
covalentes simples:
Cada átomo aporta un electrón
al enlace, es decir, se
comparte un par de electrones entre dos átomos.
·
Enlaces
covalentes dobles:
Se produce a través del
intercambio de pares de electrones entre átomos, de modo que los átomos de
adquirir configuración de gas noble (regla del octeto), que ocurre sin pérdida
o ganancia de electrones.
·
Enlaces
covalentes triples:
Cada átomo aporta tres electrones al enlace, es decir, se comparten tres pares de electrones entre dos átomos.
Cada átomo aporta tres electrones al enlace, es decir, se comparten tres pares de electrones entre dos átomos.
Propiedades de los compuestos
covalentes:
·
Se presentan en tres estados de la materia:
solio, liquido o gaseoso.
·
Los líquidos y los sólidos fundidos no
conducen la corriente eléctrica.
·
Presentan bajos puntos de fusión y de ebullición.
·
Son aislantes del calor y de la electricidad.
Geometría
Molecular Atreves de la teoría del enlace de valencia:
La geometría molecular explica
la forma que adopta las moléculas además determina las propiedades de un compuesto
como su polaridad, color, magnetismo, entre otros.
Teoría
de repulsión de los pares de electrones de la capa de valencia:
Es un modelo utilizado
en química para predecir la geometría molecular de las moléculas basada en el
grado de repulsión electrostática
de los pares de electrones.
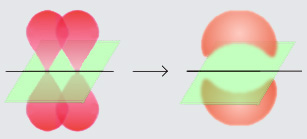
Enlace
sigma:
Es el tipo
más fuerte de enlace químico covalente, incluso más
fuerte que el enlace pi, el cual forma el doble enlace. La orbital sigma se
define de forma más clara para moléculas diatómicas usando el lenguaje y las
herramientas de la simetría de grupos.

Enlace pi:
Es un enlace covalente formado por la hibridación de dos orbitales
atómicos p. Los orbitales d también pueden participar en este tipo de enlace.
Polaridad de las moléculas:
Ocurre cundo
diferentes átomos unen, creando un enlace, por lo cual se forma un pequeño
desplazamiento de los electrones hacia el átomo más electronegativo, de esta
forma la molécula adquiere cierta polarización, que dependerá del tipo de
electronegatividad que presente en los átomos que se forman en los enlaces. Los
dos tipos que existen son: polar y no polar.
Fuerzas
intermoleculares:
Se refiere a las interacciones
que existen entre las moléculas conforme a su naturaleza. Generalmente, la
clasificación es hecha de acuerdo a la polaridad de las moléculas que están
interaccionando, o sobre la base de la naturaleza de las moléculas, de los
elementos que la conforman.
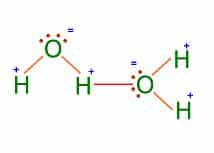
Puentes
de hidrogeno:
Es una clase de enlace que se produce a partir de
la atracción existente en un átomo
de hidrógeno y un átomo de oxígeno, flúor o nitrógeno con carga negativa.
Dicha atracción, por su parte, se conoce como interacción dipolo-dipolo y
vincula el polo positivo de una molécula con el polo negativo de otra.
Fuerzas
dipolo-dipolo:
Consiste en
la atracción electrostática entre el extremo positivo de una molécula polar y
el negativo de otra. El enlace de hidrógeno es un tipo especial de interacción dipolo-dipolo.
Fuerzas de dispersión:
Son un tipo de fuerza
intermolecular y Surgen entre moléculas
no polares, en las que pueden aparecer dipolos instantáneos. Son más intensas
cuanto mayor es la molécula, ya que los dipolos se pueden producir con más
facilidad.


Enlace
metálico:
Es un enlace químico que mantiene unidos los átomos (unión entre
núcleos atómicos y los electrones de valencia, que se juntan alrededor de éstos
como una nube) de los metales entre sí. Estos átomos se agrupan de forma muy
cercana unos a otros, lo que produce estructuras muy compactas.
Propiedades generales de los compuestos metálicos:
- Suelen ser
sólidos a temperatura ambiente.
- Tienen puntos de
fusión y ebullición muy variada (aunque suelen ser más bien alto).
- Las
conductividades térmicas y eléctricas son muy elevadas.
- Presentan brillo
metálico.
- Son muy solubles
en estado fundido en otros metales formando aleaciones.
- Son dúctiles y
maleables (no frágiles).





